
Ņ∆ńŅ£ļ ĀŪ(l®Ęi)‘ī£ļ Ó}–Õ£ļŐÓŅ’Ó}
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ(l®Ęi)‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ(l®Ęi)‘ī£ļ Ó}–Õ£ļŐÓŅ’Ó}
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ(l®Ęi)‘ī£ļ Ó}–Õ£ļŐÓŅ’Ó}
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ(l®Ęi)‘ī£ļ Ó}–Õ£ļŖxďŮÓ}
| A£ģ | ŌÚüżČA“ļ÷–Õ®»ŽŖ^(gu®į)ŃŅĶń∂Ģ—űĽĮŐľ£ļ2OH-+CO2®TCO32-+H2O | |
| B£ģ | ŌÚľÉČA»‹“ļÕ®»Ž◊„ŃŅĶń∂Ģ—űĽĮŐľ£ļCO32-+CO2+H2O®T2HCO3- | |
| C£ģ | ŌÚĻŤňŠ‚cňģ“ļ÷–Õ®»ň…ŔŃŅĶń∂Ģ—űĽĮŐľ£ļSiO32-+CO2+H2O®TH2SiO3°ż+CO32- | |
| D£ģ | ŌÚīő¬»ňŠ‚c»‹“ļ÷–Õ®»ň…ŔŃŅĶń∂Ģ—űĽĮŐľ£ļClO-+CO2+H2O®THClO+HCO3- |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ(l®Ęi)‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ(l®Ęi)‘ī£ļ Ó}–Õ£ļŐÓŅ’Ó}
| ◊Ś ÷‹∆ŕ | ĘŮA | ĘÚA | ĘůA | ĘŰA | ĘűA | ĘŲA | ĘųA | 0 |
| “Ľ | ||||||||
| ∂Ģ | A | B | C | |||||
| »ż | D | E | F | G |
 £ģ
£ģ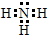 £ģ
£ģ≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ(l®Ęi)‘ī£ļ Ó}–Õ£ļŐÓŅ’Ó}
| ňŠĶńĽĮĆW(xu®¶) Ĺ ŽäŽx≥£ĒĶ(sh®ī)K | öšŃÚňŠ H2S | ĀÜŃÚňŠ H2SO3 | „tňŠ H2CrO4 | «ŤňŠ HCN |
| K1 | 9.1°Ń10-8 | 1.5°Ń10-2 | 1.8°Ń10-1 | 5.0°Ń10-10 |
| K2 | 1.1°Ń10-12 | 1.0°Ń10-7 | 3.2°Ń10-7 |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ(l®Ęi)‘ī£ļ Ó}–Õ£ļŖxďŮÓ}
| A£ģ | 5∑N | B£ģ | 6∑N | C£ģ | 2∑N | D£ģ | 8∑N |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ(l®Ęi)‘ī£ļ Ó}–Õ£ļŖxďŮÓ}
| A£ģ | FełķFeCl3»‹“ļ∑īĎ™(y®©ng)£ļFe+Fe3+®T2Fe2+ | |
| B£ģ | FełķŌ°ŃÚňŠ∑īĎ™(y®©ng)£ļ2Fe+6H+®T2Fe3++3H2°Ł | |
| C£ģ | FeCl3ŇcCl2∑īĎ™(y®©ng)£ļFe2++Cl2®TFe3++2Cl- | |
| D£ģ | Fe£®OH£©3łķŌűňŠ∑īĎ™(y®©ng)£ļFe£®OH£©3+3H+®TFe3++3H2O |
≤ťŅīīūįłļÕĹ‚őŲ>>
įŔ∂»÷¬–Ň - ĺöŃē(x®™)É‘(c®®)Ń–ĪŪ - ‘áÓ}Ń–ĪŪ
ļĢĪĪ °Ľ•¬ď(li®Ęn)ĺW(w®£ng)Ŗ`∑®ļÕ≤ĽŃľ–ŇŌĘŇeąů(b®§o)∆ĹŇ_(t®Ęi) | ĺW(w®£ng)…Ō”–ļ¶–ŇŌĘŇeąů(b®§o)Ć£(zhu®°n)Ö^(q®Ī) | Žä–Ň‘pÚ_Ňeąů(b®§o)Ć£(zhu®°n)Ö^(q®Ī) | …śöv ∑Őďüo(w®≤)÷ųŃx”–ļ¶–ŇŌĘŇeąů(b®§o)Ć£(zhu®°n)Ö^(q®Ī) | …ś∆ů«÷ôŗ(qu®Ęn)Ňeąů(b®§o)Ć£(zhu®°n)Ö^(q®Ī)
Ŗ`∑®ļÕ≤ĽŃľ–ŇŌĘŇeąů(b®§o)Žä‘í(hu®§)£ļ027-86699610 Ňeąů(b®§o)ŗ]Ōš£ļ58377363@163.com