���P���}
0 13863 13871 13877 13881 13887 13889 13893 13899 13901 13907 13913 13917 13919 13923 13929 13931 13937 13941 13943 13947 13949 13953 13955 13957 13958 13959 13961 13962 13963 13965 13967 13971 13973 13977 13979 13983 13989 13991 13997 14001 14003 14007 14013 14019 14021 14027 14031 14033 14039 14043 14049 14057 203614
��Ŀ��
��Դ��0118 �¿��}
�}�ͣ�����}
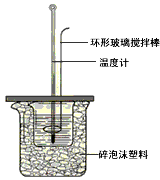
50mL 1��0 mol��L-1�}���50mL 1��1 mol��L-1�������c��Һ���D�b�����M���кͷ������������ͨ�^�y�������^�������ų��ğ�����Ӌ���к͟�������ԇ�ش����І��}
��1����С�����g��M����ĭ���ϵ�����____________________����
��2��__________����ܡ����ܡ������h(hu��n)�β���������Ğ�h(hu��n)�ν��٣����~���������ԭ����_____________________________��
��3����������粻�wӲ���������������к͟ᔵ(sh��)ֵ��Ӱ���___________���ƫ�ߡ���ƫ�͡��oӰ푡��������
��4���������60 mL 1��0 mol��L-1�}���50 mL 1��1 mol��L-1�������c��Һ�M�з������t�c�����������������ş���__________�������ӡ����������p�١���׃�������������к͟ᔵ(sh��)ֵ__________�������ӡ�������� ���p�١��� ����׃������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��������ĩ�}
�}�ͣ����x�}
���Ќ������������e�`����
A������100 g 5%��ʳ�}��Һ�r�����茢5 gʳ�}�����������������95 mLˮ�����ܽ⼴��
B������0.1 mol��L-1��������Һ�r������ȡ�ĝ������������ƿ�м�ˮϡ�
C���y�������~���w�Y(ji��)��ˮ�����r���������߅�ӟ�߅������������ֹ���w�w�R
D���к͟�y������У����íh(hu��n)�β���������p�p���ӻ��Һ
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0101 ��ĩ�}
�}�ͣ����x�}
ijͬ�W�����n�����Ҫ���������50 mL 0.50 mol/L���}���c50 mL 0.55 mol/L��NaOH ��Һ���D��ʾ���b�����M���кͷ������ͨ�^�y�������^�������ų��ğ���Ӌ���к͟����������f�����_����
A������^���П����pʧ����
B���D�Ќ���b��ȱ�٭h(hu��n)�β��������
C�������g��M�鼈�l�������ǹ̶�С����
D�����}���w�e�Ğ�60 mL������Փ�������к͟���
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0103 �����}
�}�ͣ�����}
ij���С�M�OӋ��50 mL1.0mol/L�}���50mL1.1mol/L�������c��Һ�M���кͷ��������y���к͟�������к͟�y�������P�I��Ҫ���^�ʴ_������һ�����|(zh��)������ȵ���Һ��������Ҫ�M�������^�����������������^����Ҫ�M�����������ɢʧ�������^�ʴ_�y��������ǰ����Һ�ضȵ�׃����������ش����І��}��
��1���к͟�Ĝy������IJ����x����___________��
��2��������������^����NaOH��ԭ����_____________ �����
��3���ڷ�����������зş�F(xi��n)���������HCl�]�l(f��)������t�y�õ��к͟ᔵ(sh��)ֵ___________ ����ƫ�ߡ�ƫ�ͻ�׃������
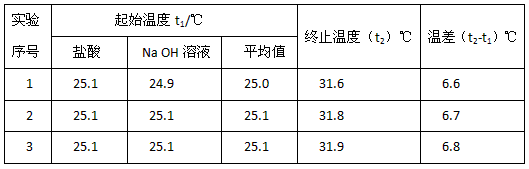
��4��ԓ���С�M�������Ό�ÿ��ȡ��Һ��50mL��������ӛ�����ԭʼ��(sh��)��(j��)��
��֪�}���������NaOH��Һ�ܶȽ��ƞ�1.00g/cm3�����кͺ���Һ�ıȟ��� C=4.18J/(g����)�tԓ�������к͟���H=_______________�������
��5�����õȝ�ȵĴ�������}���cNaOH��Һ��������t�y�õ��к͟�Ĕ�(sh��)ֵ��_________ ����ƫ��������ƫ�ͻ�׃�����������ԭ��________________ ���
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0101 �¿��}
�}�ͣ�����}
��1���к͟�y���Č��������õ��IJ����x���П����������ض�Ӌ����_________ �������__________ ���
��2����ȡ������r�����ȡ50 mL 0.50 mol�� L-1���}���������߀������ԇ����___________ ������̖����
A��50 mL 0.50 mol�� L-1 NaOH��Һ
B��50 mL 0.55 mol�� L-1 NaOH��Һ
C��1.0 g NaOH���w
��3����֪ϡ�}���cϡ�������c��Һ�������к͟ᦤH=-57.3 kJ��mol-1������Ո���x�ӷ���ʽ��ʾԓ�кͷ����ğữ�W����ʽ____________ ��
��4���F(xi��n)��һ������ϡ�������c��Һ����ϡ�������}��Һ�������ϡ��ˮ�քe��1 L 1 mol��L-1��ϡ�}��ǡ����ȫ������������䷴����քe�馤H1����H2�����H3���t��H1���������H2���������H3�Ĵ�С�Pϵ��_______________ ����
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0128 �����}
�}�ͣ�����}
50 mL1.0 mol��L-1�}���50mL1.1 mol��L-1�������c��Һ���D�b�����M���кͷ���������ͨ�^�y�������^�������ų��ğ�����Ӌ���к͟�����ԇ�ش����І��}����
�Ŵ�С�����g��M�鼈�l��������ʲô����___________________________
�ƴ�������粻�wӲ�������������к͟�Ĕ�(sh��)ֵ�к�Ӱ�? __________________________
�Ǹ���60 mL1.0mol��L-1�}���50mL1.1mol��L-1�������c��Һ�M�з����������c��������������������y�к͟�Ĕ�(sh��)ֵ��Փ���Ƿ���ȣ������]�՚��Ӱ푣��������������������__________________________
������ͬ��Ⱥ��w�e�İ�ˮ����NaOH��Һ�M�Ќ�������ʲô�y���к͟�Ĕ�(sh��)ֵƫ�ͣ�
_____________________________________________
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ����x�}
���к͟�Ĝy����������ʹ��������Ʒ���Ǟ��˜p�ٌ���`�����
A������ĭ����
B��Ӳ����
C���ض�Ӌ
D���ɂ�����
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ�����}
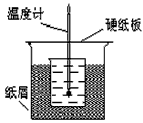
50 mL 0.50 mol��L-1�}���c 50 mL0. 55 mol��L-1 NaOH��Һ����D��ʾ���b�����M���кͷ������ͨ�^�y�������^���зų��ğ�����Ӌ���к͟���������ش����І��}��
(1)�Č���b���Ͽ����D����ȱ�ٵ�һ�N������Ʒ��_____________
(2)�����g���M�鼈�l��������_____________������
(3)�������������wӲ���壬����кͷ����ķ����ᔵ(sh��)ֵ��____________���ƫ��ƫС���oӰ푡��������
(4) NaOH��Һ�ĝ�ȴ���HCl��Һ�ĝ�ȵ�������____________ ���Ҝص���10��r�M�У������Y(ji��)��������^����`�����ԭ����______________�������к͟�Ĝy�������Ҫ�����к͟�����x���������Ϥ�������ɱM���p�ٌ���`��������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ�����}
����������D�b���M���к͟�Ĝy��������
(1)�������õăx����ԇ�����_��һ�M��( )���
A��0. 50 mol��L-1�}��������0. 50 mol��L-1 NaOH��Һ��100 mL��Ͳ1��
B��0.50 mol��L-1�}������0. 50 mol��L-1 NaOH��Һ���100 mL��Ͳ2��
C��0. 50 mol��L-1�}�������0. 55 mol��L-1 NaOH��Һ����50 mL��Ͳ1��
D��0.50 mol��L-1�}�ᣬ0. 55 mol��L-1 NaOH��Һ����50 mL��Ͳ2��
(2)���Üض�Ӌ�y������Һ�ĜضȺ���δ��ˮϴ����ֱ�Ӝy���A��Һ�Ĝض�����tӋ����ġ�H_________���ƫ��ƫС���oӰ푡������
(3)���Ӳ��ܴ_���xȡ���ǻ����Һ����ߜضȣ�____________
(4)��֪H+(aq)+OH-(aq)=H2O(l) ��H= - 57. 3kJ��mol-1��������������ݵ��w�e��������|(zh��)������ȵ�NaOH ��Һ�зքe����ϡ������������������ϡ�}����ǡ����ȫ������������������^���зų��ğ����քeӛ��Q1 kJ���Q2 kJ�������Q3 kJ�������t���ߴ�С�Pϵ��____________����Q1��Q2��Q3��ʾ��������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ�����}
ԇ�ش������к͟�y�������P���}��
(1)������ς��П�������С�ɂ�������������ĭ�� ����������ĭ���ϰ塢�h(hu��n)�β�����������0. 50 mol/L���} ��������0.55 mol/L��NaOH��Һ����ȱ�ٵČ����Ʒ��_______________���
(2)���r�����}�ἰNaOH��Һ���w�e���� 50 mL������Һ���ܶȞ�1 g/cm3������������Һ�ıȟ��� c=4. 18 J/(g����)�������ʼ�ضȞ�T1��������Kֹ�� �Ȟ�T2��������ԇ�Ɣ��к͟��Ӌ��ʽ��____________���
�鿴�𰸺ͽ���>>