
科目: 來(lái)源: 題型:

查看答案和解析>>
科目: 來(lái)源: 題型:
查看答案和解析>>
科目: 來(lái)源: 題型:
查看答案和解析>>
科目: 來(lái)源: 題型:
查看答案和解析>>
科目: 來(lái)源: 題型:
查看答案和解析>>
科目: 來(lái)源: 題型:
| 催化劑 |
| 加熱 |
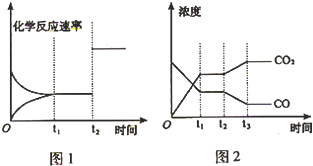
| 實(shí)驗(yàn)組 | 溫度 | 起始量 | 平衡量 | 達(dá)到平衡所需時(shí)間 | ||
| H2O | CO | H2 | CO | |||
| 1 | 650℃ | 1 mol | 2 mol | 0.8 mol | 1.2 mol | 5 min |
| 2 | 900℃ | 0.5 mol | 1 mol | 0.2 mol | 0.8 mol | 3 min |
| 3 | 900℃ | a | b | c | d | t |
查看答案和解析>>
科目: 來(lái)源: 題型:
查看答案和解析>>
科目: 來(lái)源: 題型:

查看答案和解析>>
科目: 來(lái)源: 題型:
查看答案和解析>>
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com