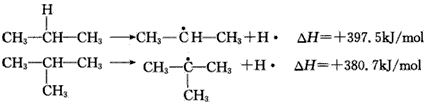���P(gu��n)��(x��)�}
0 10641 10649 10655 10659 10665 10667 10671 10677 10679 10685 10691 10695 10697 10701 10707 10709 10715 10719 10721 10725 10727 10731 10733 10735 10736 10737 10739 10740 10741 10743 10745 10749 10751 10755 10757 10761 10767 10769 10775 10779 10781 10785 10791 10797 10799 10805 10809 10811 10817 10821 10827 10835 203614
��Ŀ��
��Դ�����(xi��ng)�}
�}�ͣ����x�}
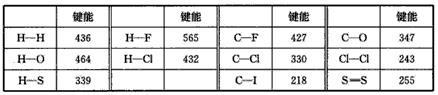
��֪����1 mol H2�����л��W(xu��)�I���ѕr(sh��)��Ҫ����436 kJ������������1 mol Cl2�����л��W(xu��)�I���ѕr(sh��)��Ҫ����
243 kJ�����������������Hԭ�Ӻ�Clԭ���γ�1 mol HCl���ӕr(sh��)ጷ�431 kJ���������������Д������_����
A�������Țⷴ��(y��ng)�����Ȼ�����w�ğữ�W(xu��)����ʽ��H2(g)��Cl2(g)��2HCl(g)
B�������Țⷴ��(y��ng)����2 mol�Ȼ�����w���������(y��ng)�Ħ�H��183 kJ��mol-1
C�������Țⷴ��(y��ng)����2 mol�Ȼ�����w������(y��ng)�Ħ�H����183 kJ��mol-1
D�������Țⷴ��(y��ng)����1 mol�Ȼ�����w����������(y��ng)�Ħ�H����183 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ������(xi��ng)�x���}
����һ��(g��)�o�����I�r(sh��)�����ĵ������Q���x��������ṩ������N��C��H�I���x���ܣ�
CH4����CH3+H�� ��H =+435. 1kJ/mol
CH3-CH2-CH2-H��CH3-CH2-CH2+H�� ��H =+410. OkJ/mol
����(j��)�ṩ��Ϣ�Д������f�������_����
A�������Ă�(g��)�x���^�̶����������^��
B���x����ԽС��C-H�IԽ�ה���������ԭ��Խ�ױ�ȡ��
C���ڹ��l���±����c�Ț�l(f��)��ȡ������(y��ng)ֻ����CH3CHClCH3
D��2-�������c�Ț�l(f��)��ȡ������(y��ng)����������ɵ�һ�ȴ���ֻ�ЃɷN
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ�����}
���W(xu��)�I���I����ָ��B(t��i)ԭ���g�γ�1mol���W(xu��)�I�r(sh��)ጷŵ��������������H(g)+I(g)��H-I(g) ��H =+297kJ/mol��H-I�I���I�ܞ�297kJ��mol-1���Ҳ����������Ɖ�1mol H-I�I��Ҫ����297kJ�ğ�����һ��(g��)���W(xu��)����(y��ng)һ�㶼���f���W(xu��)�I���Ɖĺ��»��W(xu��)�I���γ�������±���һЩ�I�ܔ�(sh��)��(j��)(kJ��mol-1)��
(1)�ɱ��Д�(sh��)��(j��)�ܷ�ó��@�ӵĽY(ji��)Փ��
�ٰ돽ԽС��ԭ���γɵĹ��r(ji��)�IԽ�ι̣����I��Խ��____����ܡ����ܡ��������
�ڷǽ�����Խ��(qi��ng)��ԭ���γɵĹ��r(ji��)�IԽ�ι�____����ܡ����ܡ���������
Ո(q��ng)�����o��(sh��)��(j��)�ҳ�һЩҎ(gu��)�������������������һ�l��____����ԇ�A(y��)�y(c��)C-Br�I���I�ܷ��� ____kJ��mol-1<C-Br�I��<___kJ��mol-1�������
(2)�ɟữ�W(xu��)����ʽH2 (g)+Cl2 (g)=2HCl(g) ��H= -185kJ��mol-1���������Y(ji��)���ϱ픵(sh��)��(j��)����֪һ��(g��)���W(xu��)����(y��ng)�ķ���(y��ng)�ᣨ�O(sh��)����(y��ng)�����������B(t��i)���c����(y��ng)�����������I��֮�g���P(gu��n)ϵ��____����� �ɟữ�W(xu��)����ʽ
2H2 (g)+S2 (s)=2H2S(g) ��H= -224. skJ��mol-1�ͱ��Д�(sh��)ֵ��Ӌ(j��)���1mol S2 (s)�⻯�r(sh��)��____(����ա��ų���)____kJ�ğ����������
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ�����}
�����ǵ�ѭ�h(hu��n)�е���Ҫ���|(zh��)��������������a(ch��n)�������������V���đ�(y��ng)�á�
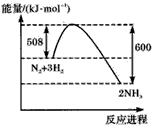
(1)�D��N2�cH2����(y��ng)�^��������׃����ʾ��D�����tԓ����(y��ng)�ğữ�W(xu��)����ʽ��___________����
( 2)��ij���W(xu��)�փ�(c��)�ϲ��N��N�I���I����948. 9kJ/mol������H-H�I���I����436.0kJ/mol���tN-H�I���I����___kJ/mol���
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ɽ�|ʡ�����}
�}�ͣ����x�}
��(du��)�����ׂ�(g��)����(y��ng)ʽ��Cl��Cl��Cl2 ��H����247kJ��mol-1 O��O��O2 ��H����493kJ��mol-1 N��N��N2 ��H����946kJ��mol-1���Եó��ĽY(ji��)Փ��
A���ڳ����µ�?d��)�������������Țⶼ��(w��n)��
B��������������ȵĆ��|(zh��)��������w
C�����������������ȵĆ��|(zh��)��������������(qi��ng)
D����?d��)������������Ț���ܶȲ��?
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0115 �����}
�}�ͣ����x�}
��֪1 g�����ȫȼ������ˮ����r(sh��)�ų�����121 kJ�������������1 mol O��O�I��ȫ���ѕr(sh��)���՟���496 kJ�������ˮ������1 mol H��O�I�γɕr(sh��)�ų�����463 kJ�����t�����1mol H��H�I���ѕr(sh��)���՟�����
A��920 kJ
B��557 kJ
C��436 kJ
D��188 kJ
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0101 �����}
�}�ͣ����x�}
��֪���� 1molH2�����л��W(xu��)�I���ѕr(sh��)��Ҫ����436kJ����������� 1molCl2�����л��W(xu��)�I���ѕr(sh��)��Ҫ����
243kJ������������ ��Hԭ�Ӻ�Clԭ���γ�1molHCl���ӕr(sh��)ጷ�431kJ��������������Д������_����
A��1��(g��)����Ӻ�1��(g��)�ȷ��ӷ���(y��ng)����1��(g��)�Ȼ�������������(y��ng)�ġ�H��-183kJ��mol-1
B������c�Țⷴ��(y��ng)����2mol�Ȼ�����w�����������(y��ng)�ġ�H��183kJ��mol-1
C������c�Țⷴ��(y��ng)����2mol�Ȼ�����w����������(y��ng)�ġ�H��-183kJ��mol-1
D������c�Țⷴ��(y��ng)����1mol�Ȼ�����w������(y��ng)�ġ�H��-183kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ������ʡ�߿����}
�}�ͣ����x�}
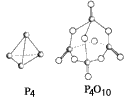
�����c����ɰl(f��)�����·���(y��ng)��P4��5O2��P4O10����֪�������л��W(xu��)�I��Ҫ���յ������քe�飺P-P a kJ��mol��1���P-O b kJ��mol��1��P===O c kJ��mol��1����O===O d kJ��mol��1�����������(j��)�Dʾ�ķ��ӽY(ji��)��(g��u)�����P(gu��n)��(sh��)��(j��)����ԓ����(y��ng)�Ħ�H����������_����
A��(6a��5d��4c��12b) kJ��mol��1
B��(4c��12b��6a��5d) kJ��mol��1
C��(4c��12b��4a��5d) kJ��mol��1
D��(4a��5d��4c��12b) kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��0115 �¿��}
�}�ͣ����x�}
��֪��
��1mol H2�����л��W(xu��)�I���ѕr(sh��)��Ҫ����436kJ������
��1mol Cl2�����л��W(xu��)�I���ѕr(sh��)��Ҫ����243kJ������
����Hԭ�Ӻ�Clԭ���γ�1mol HCl���ӕr(sh��)ጷ�431kJ������
���������_����
A�������Țⷴ��(y��ng)�����Ȼ�����w�ğữ�W(xu��)����ʽ�� H2(g)+Cl2(g)��2HCl(g)��H��-183kJ/mol
B�������Țⷴ��(y��ng)����2mol�Ȼ�����w������(y��ng)�ġ�H��183kJ/mol
C������c�Țⷴ��(y��ng)�����Ȼ�����w�ķ���(y��ng)�����ᷴ��(y��ng)
D�������Țⷴ��(y��ng)����1mol�Ȼ�����w���������(y��ng)�ġ�H��-183kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ����x�}
���W(xu��)����(y��ng)��ҕ���f�I���Ѻ����I�γɵ��^�����������r(ji��)�I���I���ǃɷNԭ���g�γ�1mol���r(ji��)�I���������^�̣��r(sh��)ጷţ������գ���������������֪H-H�I���I�ܞ�436kJ/mol�� Cl-Cl�I���I�ܞ�243kJ/mol����H-Cl�I���I�ܞ�431kJ/mol����t H2(g) +Cl2(g)=2HCl(g)�ķ���(y��ng)�ᣨ��H������
A.- 183kJ/mol
B.+183kJ/mol
C.- 862kJ/mol
D.+862kJ/mol
�鿴�𰸺ͽ���>>