
科目: 來源: 題型:實驗探究題
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:推斷題
| 食物 | 蘋果 | 葡萄 | 牛奶 | 玉米 |
| PH | 2.9~3.3 | 3.5~4.5 | 6.3~6.6 | 6.8~8.0 |
查看答案和解析>>
科目: 來源: 題型:實驗探究題

| Mg2+ | Fe2+ | Fe3+ | |
| 開始沉淀 | 9.4 | 7.9 | 2.7 |
| 沉淀完全 | 12.4 | 9.6 | 3.7 |
查看答案和解析>>
科目: 來源: 題型:實驗探究題

查看答案和解析>>
科目: 來源: 題型:實驗探究題
 某制備氫氣新工藝的主要流程如下:
某制備氫氣新工藝的主要流程如下:查看答案和解析>>
科目: 來源: 題型:實驗探究題
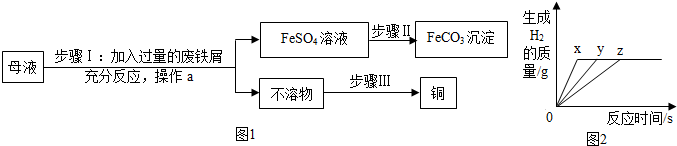
查看答案和解析>>
科目: 來源: 題型:實驗探究題
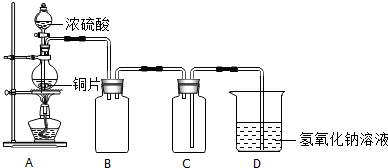
查看答案和解析>>
科目: 來源: 題型:推斷題
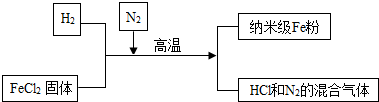
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com