
�}Ŀ�б�(�����𰸺ͽ���)
| ��x�ܣ�kJ/mol�� | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| ������ |
| �� |
| ������ |
| �� |
| B |
|
C |
|
���T������ |
| һ���l�� |
| һ���l�� |
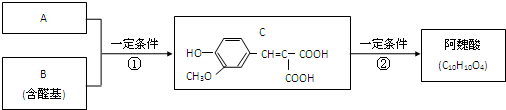
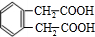
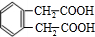
 +3Na2CO3��+3NaHCO3
+3Na2CO3��+3NaHCO3 +3Na2CO3��+3NaHCO3
+3Na2CO3��+3NaHCO3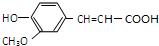
| һ���l�� |

| һ���l�� |

| 127bc��10-3 |
| 6a |
| 127bc��10-3 |
| 6a |
c
| ||
| c(I2)?c2(I-) |
c
| ||
| c(I2)?c2(I-) |
| KI��ʼ���/mol?L-1 | 0.02 | 0.04 | 0.06 | 0.08 | 0.10 |
| I3-% | 88.98 | 88.04 | 85.28 | 82.26 | 79.23 |
| I42-% | 4.38 | 8.67 | 12.60 | 16.21 | 19.53 |
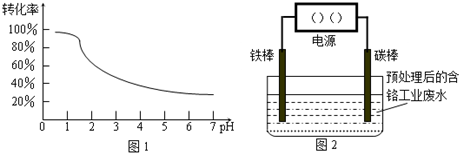
| ������ | Fe��OH��3 | Fe��OH��2 | Cr��OH��3 | Al��OH��3 |
| �_(k��i)ʼ���� | 2.7 | 7.5 | 4.3 | 3.4 |
| ��ȫ���� | 4.1 | 9.7 | 5.6 | 5.2 |
| +6 |
| Cr |
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com