���P(gu��n)��(x��)�}
0 7574 7582 7588 7592 7598 7600 7604 7610 7612 7618 7624 7628 7630 7634 7640 7642 7648 7652 7654 7658 7660 7664 7666 7668 7669 7670 7672 7673 7674 7676 7678 7682 7684 7688 7690 7694 7700 7702 7708 7712 7714 7718 7724 7730 7732 7738 7742 7744 7750 7754 7760 7768 203614
��Ŀ��
��Դ������ʡģ�M�}
�}�ͣ����x�}
���ÉA����������Һ�������������������F�����γ�һ��Fe3O4(Ҳ�ɱ�ʾ��FeFe2O4)��Ĥ�������o��(n��i)���������ܸ��g��������@�N�����������{�������{�r�l(f��)�����·���(y��ng)��
��3Fe��NaNO2��5NaOH===3Na2FeO2��H2O��NH3��
��Na2FeO2��NaNO2��H2O===Na2Fe2O4��NH3����NaOH(δ��ƽ)
��Na2FeO2��Na2Fe2O4��2H2O===Fe3O4��4NaOH
�����f�������_����
A��Fe3O4�ȿɿ������������������ֿɿ������F�}
B������(y��ng)����ƽ������H2O�Ļ��W(xu��)Ӌ����(sh��)��3
C������(y��ng)����������Na2Fe2O4������������Na2FeO2��߀ԭ��
D���A�ԗl��������NaNO2�������Ա�Na2FeO2���Na2Fe2O4����
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ���Ĵ�ʡģ�M�}
�}�ͣ����x�}
��CuSO4��Һ����μ����^��KI��Һ���^�쵽�a(ch��n)����ɫ�������������Һ׃?y��u)���ɫ����������?y��ng)��Ļ�����в���ͨ��SO2���w�����Һ��u׃�ɟoɫ���t�����f�����_����
A.��ɫ������CuI2���������ɫ��Һ����I2
B.�μ�KI��Һ�r���D(zhu��n)��1mol��ӕr����1mol��ɫ����
C.ͨ��SO2�r������SO2�cI2����(y��ng)��I2��߀ԭ��
D.�������l����������|(zh��)�������ԣ�I2>Cu2+>SO2
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ������ʡģ�M�}
�}�ͣ����x�}
�ڝ��}����H3AsO3�cSnCl2����(y��ng)���x�ӷ���ʽ��3SnCl2+12Cl-+2H3AsO3+6H+==2As+3SNCl62- + 6M���P(gu��n)��ԓ����(y��ng)���f�������_�ĽM����
����������H3AsO3 ��߀ԭ�ԣ�Cl->As ��ÿ����1 mol As��������(y��ng)���D(zhu��n)����ӵ����|(zh��)������3 mol ��M��OH- ��SnCl62-�������a(ch��n)��
A.�٢ڢܢ�
B.�٢ۢ�
C.�٢ڢۢ�
D��ֻ�Т٢�
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ɽ�|ʡ�¿��}
�}�ͣ����x�}
R�����X�����Y��Z���ķNԪ�أ��䳣Ҋ���σr���飫2�r�����X2���c���|(zh��)R������(y��ng)��X2����Z��X��Z2������Y��Z2����Y(ji��)2����Z������@�ķN�x�ӱ�߀ԭ��0�r�r���F(xi��n)�������Դ�С����
A.R2����X2����Z2����Y2��
B.X2����R2����Y2����Z2��
C.Y2����Z2����R2����X2��
D.Z2����X2����R2����Y2��
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ɽ�|ʡ�¿��}
�}�ͣ����x�}
��֪2FeCl3��2KI=2FeCl2��2KCl��I2���H2S��I2=2HI��S����������Д������_����
A������������Fe3����I2��S
B��������I2��S��Fe3��
C�������߀ԭ��Fe2����I����H2S
D������߀ԭ��Fe2����H2S��I��
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ɽ�|ʡ�¿��}
�}�ͣ����x�}
��֪����(y��ng)��
��2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O
��K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O
��Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4
���нY(ji��)Փ���_����
A���٢ڢ۾�������߀ԭ����(y��ng)
B�������ԏ�������ǣ�K2Cr2O7��Fe2(SO4)3��I2
C������(y��ng)�����������c߀ԭ�������|(zh��)����֮�Ȟ�6��1
D������(y��ng)����0.1mol߀ԭ����ʧȥ��Ӕ�(sh��)��1.2��1022
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ���㽭ʡģ�M�}
�}�ͣ����x�}
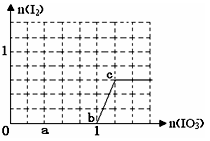
��֪��߀ԭ��HSO3->I-��������IO3-> I2������ں� 0.3 mol NaHSO3����Һ����μ���KIO3��Һ��������KIO3������I2�����|(zh��)�������P(gu��n)ϵ������D��ʾ��������f�������_����
A��0~b�g�ķ���(y��ng)���������x�ӷ���ʽ��ʾ��3HSO3- + IO3-��3SO42- + I- + 3H+
B��a(ch��n)�c�r����NaHSO3�����|(zh��)������0.12 mol
C��b�c�r��߀ԭ�a(ch��n)�������KI��NaI�������b~c�g��߀ԭ�a(ch��n)����I2
D����(d��ng)��Һ��I-�cI2�����|(zh��)����֮�Ȟ�5��2�r��������KIO3��0.18mol
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ����x�}
�F(xi��n)��M��N��P����E 4�NԪ�صĆ��|(zh��)�����ܰl(f��)�����·���(y��ng)��
����ˮ��Һ������M��N2��===M2����N��
��P��2H2O(��)===P(OH)2��H2����
��N����E���B����ϡH2SO4������늘O����(y��ng)�飺N��2e��===N2�����2H����2e��===H2��
�Д�������߀ԭ���ɏ������������
A��M��N�����P�����E
B��P��M���N��E
C��M����N�����E������P
D��E��P����M����N
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ����x�}
��SO2���w�c����Fe2(SO4)3��Һ��ȫ����(y��ng)������ټ���K2Cr2O7��Һ����l(f��)�����ɂ����W(xu��)����(y��ng)�� SO2��2Fe3����2H2O===SO42����2Fe2����4H��
Cr2O72����6Fe2����14H��===2Cr3����6Fe3����7H2O
�������P(gu��n)�f�����_����
A��߀ԭ��Cr3��>Fe2��>SO2
B��������Cr2O72��>SO2>Fe3��
C��Cr2O72���܌�Na2SO3������Na2SO4
D���ɂ�����(y��ng)��Fe2(SO4)3����߀ԭ��
�鿴�𰸺ͽ���>>
��Ŀ��
��Դ��ͬ���}
�}�ͣ�����}
ij����(y��ng)�з���(y��ng)���c�������У�AsH3��H2SO4������KBrO3��K2SO4�������H3AsO4������H2O��һ�Nδ֪���|(zh��)X.
(1)��֪KBrO3�ڷ���(y��ng)�еõ���ӣ��tԓ����(y��ng)��߀ԭ����______________________��
(2)��֪0.2mol KBrO3�ڷ���(y��ng)�еõ�1mol�������X����tX�Ļ��W(xu��)ʽ��______________��
(3)����(j��)��������(y��ng)����֪________________��
a�������ԣ�KBrO3>H3AsO4 b�������ԣ�H3AsO4>KBrO3 c��߀ԭ�ԣ�AsH3>X d��߀ԭ�ԣ�X>AsH3
(4)����������߀ԭ���Ļ��W(xu��)ʽ������ƽ���ϵ��(sh��)�������з����У����˳�����D(zhu��n)�Ƶķ���͔�(sh��)Ŀ��______+_____
�鿴�𰸺ͽ���>>