
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ����x�}
| A�� | �а�ɫ�������� | B�� | �](m��i)�г������� | ||
| C�� | �мt��ɫ�������� | D�� | �Пo(w��)ɫ���w�a(ch��n)�� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��x���}
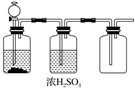
| A�� | FeS��ϡH2SO4 | B�� | �ӟ�NaCl�͝�H2SO4��HCl | ||
| C�� | ����ʯ��ϡ�}�� | D�� | MnO2�͝��}�� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ��Ɣ��}
 ��C�cˮ����(y��ng)�Ļ��W(xu��)����ʽ��2Na2O2+2H2O=4NaOH+O2����
��C�cˮ����(y��ng)�Ļ��W(xu��)����ʽ��2Na2O2+2H2O=4NaOH+O2�����鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ����x�}
| A�� | ������|(zh��)�����W(xu��)�I | |
| B�� | ���зǘO���I�Ļ����ﲻһ���ǹ��r(ji��)������ | |
| C�� | ����(y��ng)�ᅡ�������������ᅡ�����ķ���(y��ng)һ�������ᷴ��(y��ng) | |
| D�� | �ɷǽ���Ԫ�ؘ�(g��u)�ɵĻ�����һ���ǹ��r(ji��)������ |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
| ��(sh��)�(y��n)��̖(h��o) | �� | �� | �� | �� |
| ϡ�����w�e/mL | 100 | 200 | 300 | 400 |
| ʣ������|(zh��)��/g | 9.0 | 4.8 | 0 | 0 |
| NO�w�e/L | 1.12 | 2.24 | 3.36 | V |
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ���(sh��)�(y��n)�}
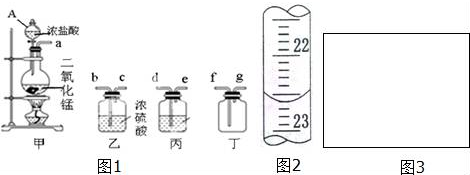
�鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ���(sh��)�(y��n)�}
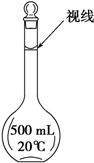 ��(sh��)�(y��n)������500mL 0.2mol/L��FeSO4��Һ����(sh��)�(y��n)�������E�У�
��(sh��)�(y��n)������500mL 0.2mol/L��FeSO4��Һ����(sh��)�(y��n)�������E�У��鿴�𰸺ͽ���>>
��Ŀ�� ��(l��i)Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com