
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | ���I�ǻ��W�I | |
| B�� | ������cˮ�γɚ��I | |
| C�� | �Ҵ����Ӹ�ˮ����֮�g���ڷ����A���͚��I | |
| D�� | �⻯��ķ��c���Ȼ���ķ��c�������ڵ⻯�����֮�g���ښ��I |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}

�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
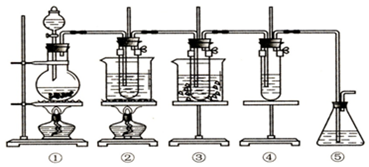
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}

| ������ȼ���ėl�� | ��ȼ���F���� | |||
| ��̖ | �ἃ�wϵ�ض�/�� | ����EDTA�|(zh��)��/g | ���뱣�U���|(zh��)��/g | W��Fe��/��10-4g�� |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| ��̖ | c��HA��/mol•L-1 | c��NaOH��/mol•L-1 | �����Һ��pH |
| �� | 0.1 | 0.1 | pH=a |
| �� | 0.2 | 0.2 | pH=9 |
| �� | c1 | 0.2 | pH=7 |
| �� | 0.2 | 0.1 | pH��7 |
| A�� | c1=0.2 | |
| B�� | ���M���Һ��c��Na+����c��A-����c��H+����c��OH-�� | |
| C�� | a��9 | |
| D�� | ���ҽM���Һ����ˮ��x����c��OH-��=10-5mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | ÿ��ˮ���Ӄ�(n��i)���Ѓɂ����I | |
| B�� | ֻҪ�К�Ԫ�ؾ����γɚ��I | |
| C�� | �����g���γɚ��Iʹ���|(zh��)�����c�ͷ��c���� | |
| D�� | HF�ķ�(w��n)���Ժ��������������g���γɚ��I |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | �ٺ͢� | B�� | �� | C�� | �ۺ͢� | D�� | ���϶����� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | 3.36 L | B�� | 4.48 L | C�� | 5.6 L | D�� | 6.72 L |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | NaOH | B�� | H2SO4 | C�� | Na2CO3 | D�� | Na2SO4 |
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com