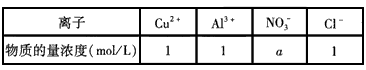���P(gu��n)��(x��)�}
0 12305 12313 12319 12323 12329 12331 12335 12341 12343 12349 12355 12359 12361 12365 12371 12373 12379 12383 12385 12389 12391 12395 12397 12399 12400 12401 12403 12404 12405 12407 12409 12413 12415 12419 12421 12425 12431 12433 12439 12443 12445 12449 12455 12461 12463 12469 12473 12475 12481 12485 12491 12499 203614
��Ŀ��
��(l��i)Դ��ģ�M�}
�}�ͣ�����}
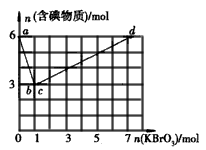
�F(xi��n)��6 mol KI��������Һ����μ���KBrO3��Һ�������(g��)�^(gu��)���к������|(zh��)�����|(zh��)�����c������KBrO3�����|(zh��)�������P(gu��n)ϵ��D��ʾ���������֪��
��BrO3-+6I-+6H+=3I2+Br-+3H2O;
��2BrO3-+I2=2IO3-+Br2�������
Ո(q��ng)�ش����І�(w��n)�}��
(1)b�c(di��n)�r(sh��)����KI����(y��ng)��ȫ��������t���ĵ��������c߀ԭ�������|(zh��)����֮�Ȟ�_(k��i)__��߀ԭ�a(ch��n)����___ �����
(2)b��c�^(gu��)����ֻ��һ�NԪ�صĻ��σr(ji��)�l(f��)����׃������(xi��)��ԓ�^(gu��)���аl(f��)������(y��ng)���x�ӷ���ʽ__������
(3)��ͬ�W(xu��)�ɷ���(y��ng)�ڵó�������I2>Br2�ĽY(ji��)Փ����������J(r��n)���Ƿ����_�������f(shu��)������___��
(4)��6 mol KI��������Һ��������n(KBrO3)�����ֵ��_(k��i)_�����
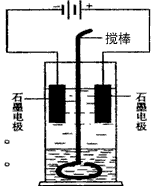
(5)�F(xi��n)��늽ⷨ�Ƃ����⛣���(sh��)�(y��n)�b����D��ʾ�������Ȍ�һ�����ĵ����� �^(gu��)�����������Һ���������l(f��)������(y��ng)��3I2+6KOH=5KI+KIO3+3H2O������ ��ԓ��Һ�����(y��ng)�O�^(q��)�����팢���������Һ����ꎘO�^(q��)�������_(k��i)ʼ늽���������(y��ng)�O��늘O����(y��ng)ʽ��_(k��i)__������ꎘO�^(gu��n)�쵽�ĬF(xi��n)����___�����
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ģ�M�}
�}�ͣ����x�}
�w�e��1 L��ij��Һ�к��е��x�Ӽ��������±���ʾ����� ��������Һ�в������늘Oͨ�늽�����������늽�r(sh��)��Һ�w�e��׃����늘O�a(ch��n)����ܴ��ڵ��ܽ�F(xi��n)��(d��ng)�·����3 mol e-ͨ�^(gu��)�r(sh��)���������f(shu��)�����_����
A��늽����Һ��pH =0
B��a(ch��n)=3
C���(y��ng)�O����1.5 mol Cl2
D��ꎘO�����Ľ������~�c�X
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��0108 �¿��}
�}�ͣ����x�}
늽�ϡH2SO4����Cu(NO3)2������NaCl�Ļ��Һ���������һ�Εr(sh��)�gꎘO���(y��ng)�O�Ϸքe���������|(zh��)�քe��
A�����H2��Cl2
B������Cu��Cl2
C��H2��O2
D����Cu��O2
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��0108 �¿��}
�}�ͣ����x�}
��ʯī��늘O늽�2 mol��L-1NaCl��1 mol��L-1MgSO4�����Һ�r(sh��)�����������(xi��n)��������
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��0108 �¿��}
�}�ͣ�����}
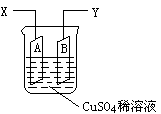
��D�ǿ����ڜy(c��)�������ӵ��_����(sh��)���b��ʾ��D�������A�Ǽ��~Ƭ������B��ʯī���������100mLCuSO4ϡ��Һ�У��~Ƭ����ʯī�c������(d��o)��(xi��n)���B�����������˷քe��X�����Y��
(1) ��(d��ng)��IA�����늽�6min����������y(c��)���~ƬA���|(zh��)���p����2.56g����� �t�D�b���е�X�ˑ�(y��ng)�cֱ��늵�________�O���B����
(2)늽���Դ���������2IA�����늽�6min����������O(sh��)��Һ�w�e��׃�����y(c��)����Һ��CuSO4���|(zh��)������Ȟ�0.1mol/L������tԭ��Һ��CuSO4���|(zh��)�������________mol/L���������Һ��H+�����|(zh��)������Ȟ�_(k��i)______mol/L��
(3)��ʽӋ(j��)�㌍(sh��)�(y��n)�y(c��)�õİ����ӵ��_����(sh��)NA����I��ʾ��_________mol-1���������֪������e=1.60��10-19C��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ���߿����}
�}�ͣ�����}
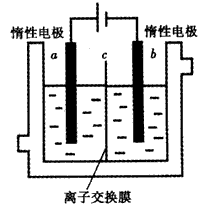
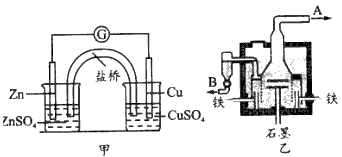
�ڲ����AͲ��ʢ�ЃɷN�o(w��)ɫ�Ļ������ܵ�����Һ�w����ό�Һ�w�в���ɸ�ʯī늘O���AͲ��(n��i)߀����һ���¶ˏ��ɭh(hu��n)��IJ����������������������(d��ng)Һ�w��������b�����D��������ͨ�Դ������(y��ng)�O��?ch��)���Һ�w�ʬF(xi��n)��ɫ�����ɫ�ɜ\׃�����ꎘO���К������ɡ�ֹͣͨ����ȡ��늘O���Ô��������Ҕ���(d��ng)��������o�ú�Һ�w�ֳַɃɌ�������Һ�w���ϼtɫ������ό�Һ�w���o(w��)ɫ������
����(j��)������(sh��)�(y��n)�ش�
��1���(y��ng)�O�ϵ�늘O����(y��ng)ʽ��_(k��i)___________����
��2��ꎘO�ϵ�늘O����(y��ng)ʽ��_(k��i)___________�������
��3��ԭ�ό�Һ�w��____________________�������
��4��ԭ��Һ�w��____________________������
��5�������Ɍ�Һ�w�ɫ�l(f��)��׃����ԭ����____________________
��6��Ҫ�z�(y��n)�ό�Һ�w�к��еĽ����x���������䷽����________��������F(xi��n)����____________���
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ������(xi��ng)�x���}
�܉�ʹ����(y��ng)Cu +2H2O=Cu(OH)2+ H2���l(f��)������
A���~Ƭ��ԭ늳ص�ؓ(f��)�O������̼����ԭ늳ص����O���Ȼ��c��늽��|(zh��)��Һ
B���~�\�Ͻ��ڳ���Ŀ՚��аl(f��)��늻��W(xu��)���g
C�����~Ƭ��ꎡ��(y��ng)늘O������늽��Ȼ��c��Һ
D�����~Ƭ��ꎡ��(y��ng)늘O�����늽������~��Һ
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ����x�}
��D����ʾ���\�~ԭ늳��b�ã��Ҟ�늽������Ȼ��c�b����������t�����f(shu��)�����_����
A�����b�����\��ؓ(f��)�O�������l(f��)��߀ԭ����(y��ng)���~�����O����l(f��)����������(y��ng)
B�����b���}���������ʹ����(y��ng)�^(gu��)����ZnSO4��Һ��CuSO4��Һ���������
C�����b�����F�O��늘O����(y��ng)ʽ�飺2Na - 2e -= 2Na+
D�����b����B���Ț��������A���c����
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ����x�}
���P(gu��n)X�������Y�������Z��W�ķN���ٵČ�(sh��)�(y��n)���£� ����(j��)������(sh��)����������Д���Ɯy(c��)�e(cu��)�`����
A.Z���(y��ng)�x���������(qi��ng)
B.W��߀ԭ�ԏ�(qi��ng)��Y��߀ԭ��
C.Z����CuSO4��Һ��һ����Cu����
D.��Y����Z��ϡ����ɘ�(g��u)��ԭ늳������Y��ؓ(f��)�O
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��ͬ���}
�}�ͣ����x�}
��1 L pH =5��CuSO4��Һ�ö���늘O늽�һ�Εr(sh��)�g����Һ��pH׃?y��u)?����ʹ��Һ�ĝ��������pH�c늽�ǰ��ͬ������ɲ��õķ�����
A������Һ�м���0.49 gCu(OH)2
B������Һ�м���0. 62 g CuCO3
C������Һ�м���0. 32 gCuO
D������Һ�м���0. 80 g CuSO4
�鿴�𰸺ͽ���>>