
��Ŀ�� ��Դ�� �}�ͣ���x����

| ||
| ||
| ��̖ | �Q���� | ����ǰ | ��ӳ�� |
| һ | Ӳ�|�����ܼ���ʢ���w���|�� | 76.2g | 73.8g |
| �� | C�b�ÿ��|�� | 153.7g | 160.3g |
| ||
| 160 |
| 132 |
| X |
| 6.6g |
| 8g |
| 10g |
| ||
| 160 |
| 132 |
| X |
| 6.6g |
| 8g |
| 10g |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
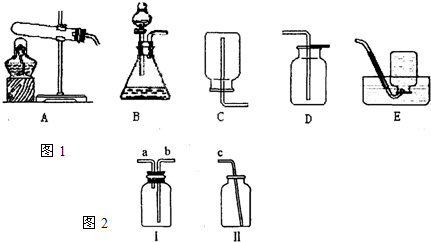
| ||
| �� |
| ||
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
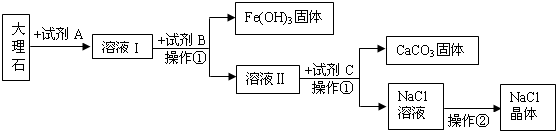
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ���x����

�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
| ��̖ | ��1�� | ��2�� | ��3�� | ��4�� | ||||||||
| ���Q | ������ | �ʚ� | ���������F | �Aʽ̼���~�����~�G�� �Aʽ̼���~�����~�G�� | ||||||||
| ���Wʽ | H2
|
|
|
Cu2��OH��2
| ||||||||
| e | �� | ���| ���| |
�A �A |
�} | ||||||||
| ���σr | +4 +4 |
0 | +2 | +4 |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�
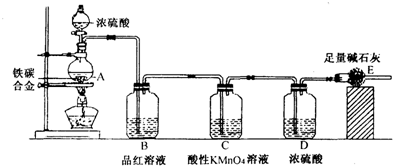
�鿴�𰸺ͽ���>>
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com